### PONTOS CHAVE
- Sempre é importante lembrar de otimizar medidas de controle pressórico, uso de IECA/BRA e mudança do estilo de vida (restrição sódio na dieta, parar tabagismo, controle de peso e realização de atividade física).
- O tratamento imunossupressor fica reservado para os pacientes de alto risco de progressão de doença renal.
- Consideramos pacientes de alto risco aqueles com proteinuria ≥1 g/dia a despeito de tratamento de suporte otimizado por > 3 meses.
- Seguindo o TESTING Trial 2022: para pacientes com proteinúria acima de 1g, realizamos o esquema com dose reduzida, o equivalente a prednisona 0,5mg/kg até o máximo de 40mg/d, com desmame de 5 mg ao mês).
[Finalmente, devemos ou não usar corticoides em paciente com nefropatia por IgA (NIgA) de alto risco?](#)
###### Essa pergunta sempre nos vem a cabeça já que, após 2 grandes trials realizados em 2015 o [STOP IgA](https://www.nejm.org/doi/full/10.1056/NEJMoa1415463) e o [Testing trial](https://jamanetwork.com/journals/jama/fullarticle/2646717) em 2017 trouxeram dúvidas sobre os riscos relacionados à esta terapia.
**Vamos relembrar os trials anteriores bem rapidamente?**
[**STOP IgA**](https://www.nejm.org/doi/full/10.1056/NEJMoa1415463)
Neste estudo 162 pacientes de alto risco (proteinúria 0,75-3.5g e com TFG > 30mL / min / 1.73m2, mesmo após tratamento de suporte por 6 meses) foram randomizados para receber terapia de suporte ou terapia imunossupressora por 3 anos.
- Terapia de suporte: inibidores do sistema renina angiotensina aldosterona e controle da hipertensão < 125 x 75mmHg
- Terapia imunossupressora
- **TFGe > 60mL/min/1.73m2:** 6 meses (metilprednisolona, administrada por via intravenosa na dose de 1 g por dia durante 3 dias no início dos meses 1, 3 e 5; e prednisolona oral na dose de 0,5 mg por quilo por 48 horas nos outros dias)
- **TFGe > 30-59 mL/min/1.73m2** : ciclofosfamida oral 1,5 mg/kg/d por por 3 meses, seguido de azatioprina na dose de 1,5mg/kg/d durante os meses 4 a 36, mais prednisolona oral na dose de 40 mg por dia, reduzido para 10 mg por dia, ao longo os primeiros 3 meses, 10 mg por dia durante os meses 4 a 6, e 7,5 mg por dia durante os meses 7 a 36
O **desfecho primário** era remissão clínica completa: relação proteína-creatinina <0,2 e uma diminuição TFGe de < 5 mL/min/1,73 m2 a partir da linha de base e uma diminuição na TFGe < 15mL/min/1,73 m2 no final do estudo.
Os resultados deste estudo mostraram:
- 4 pacientes apresentaram remissão clínica completa (5%) no grupo de cuidados de suporte, em comparação com 14 (17%) no grupo de imunossupressão (P = 0,01).
- Mas 28% no tratamento de suporte e 26% no grupo de imunossupressão tiveram uma diminuição na TFGe de pelo menos, menos 15 mL /min/ 1,73 m2 (P=0,75).
- Não houve diferença significativa no declínio anual na TFG entre os dois grupos.
- O pior (e esperado), mais pacientes no grupo de imunossupressão do que no grupo de cuidados de suporte tiveram infecções graves, hiperglicemia, e ganho de peso superior a 5 kg no primeiro ano de tratamento e um paciente no grupo de imunossupressão morreu de sepse.
A conclusão foi que **a adição de terapia imunossupressora aos cuidados intensivos de suporte em pacientes com NIgA de alto risco não melhorou significativamente os desfechos**, e durante o período de 3 anos do estudo, mais efeitos adversos foram observados entre os pacientes que receberam terapia imunossupressora, sem alteração na queda da TFGe. Ou seja, houve melhora na proteinúria sem melhora na TFGe.
[**TESTING**](https://jamanetwork.com/journals/jama/fullarticle/2646717)
Este ensaio clínico randomizado, multicêntrico, duplo-cego, placebo controlado, avaliou pacientes com NIgA que mantinham proteinúria >1g e TFGe 20-100 mL/min/1,73 m2 após o controle com IECA/BRA e da hipertensão por 3 meses.
Neste estudo os pacientes foram randomizados 1:1 para iniciar metilprednisolona oral (0,6-0,8 mg/kg/d; máximo, 48 mg/d) ou placebo correspondente por 2 meses, com subsequente desmame de 4 a 6 meses.
O desfecho composto primário foi TFGe < 15mL/min/1.73m2, morte por doença renal ou diminuição de 40% na TFGe de base. Os Resultados de segurança predefinidos foram infecção grave, diabetes _de novo_, hemorragia gastrointestinal, fratura/osteonecrose e eventos cardiovasculares. O seguimento médio necessário foi estimado em 5 anos.
No entanto, após a randomização de 262 participantes o recrutamento foi descontinuado devido ao excesso de eventos adversos graves que ocorreram em 20 participantes (14,7%) do grupo metilprednisolona vs 4 (3,2%) em o grupo placebo (P = 0,001), principalmente devido a excesso de infecções graves, incluindo 2 mortes.
No entanto, o desfecho renal primário ocorreu em 8 participantes (5,9%) em o grupo metilprednisolona vs 20 (15,9%) no grupo placebo (P = 0,02). Como conclusão deste estudo tivemos que, entre os pacientes com NIgA e proteinúria de 1 g/dia ou mais, a metilprednisolona oral foi associada a um risco aumentado de eventos adversos, principalmente infecções. Embora os resultados tenham sido consistentes com potencial benefício, conclusões definitivas sobre o benefício do tratamento não podem ser feitas, devido à encerramento do julgamento.
Agora vem o [**TESTING trial**](https://jamanetwork.com/journals/jama/fullarticle/2792252)
A partir destes resultado, os investigadores modificaram o protocolo, e os participantes foram randomizados, posteriormente, em uma proporção de para receber **metilprednisolona oral 0,4 mg/kg/d, máximo 32mg/d, desmame de 4mg/d/mês e adição de profilaxia antibiótica para pneumonia por Pneumocystis para participantes subsequentes (sulfametoxazol trimetoprim 400/80mg)**
**O tratamento completo durava de 6-9meses a depender da dose inicial.** O desfecho primário foi um composto de **declínio de 40% na TFGe, insuficiência renal (diálise, transplante) ou morte devido a doença renal**. A TFGe g mínima passou a ser 30mL/min/1.73m2. Após recrutarem 262 pacientes até 2017, os pesquisadores decidiram recrutar mais 240 participantes para receber o novo esquema.
No resultado conjunto (2012- 2019), um total de 950 potencialmente pacientes elegíveis foram rastreados em 67 locais da Austrália (6 locais), Canadá (8 locais), China (41 locais), Índia (6 locais) e Malásia (6 locais). No geral, **503 participantes foram randomizados** (257 para o grupo metilprednisolona e 246 para o grupo placebo grupo), incluindo **262 com base no protocolo original de dose completa e 241 com base no protocolo de dose reduzida.**
A média de idade dos participantes foi de **38 anos**, 39% eram mulheres, a média da TFG inicial era **61,5 mL/min/1,73m2** e média da **proteinúria de 24 horas de 2,46 g por dia**. Em comparação com os inscritos para a coorte de dose completa, os participantes da coorte de dose reduzida eram menos prováveis de serem da China (95% vs 51%) e tinham uma maior índice de massa corporal, maior TFGe, um tempo médio mais longo desde biópsia renal diagnóstica e menos atrofia tubular e fibrose nessa biópsia. Os pacientes foram acompanhados por uma média de 4.2 anos (5.7 dose elevada e 2.6 anos dose reduzida).
O desfecho primário ocorreu com menos frequência no grupo metilprednisolona do que o grupo placebo (74 [28,8%] vs 106 [43,1%]; HR, 0,53 [IC 95%, 0,39-0,72]; P < 0,001; com diferença de taxa de evento anual, **−4,8% ao ano** [IC 95%, −8,0% a −1,6%] **(Figura A).**
O risco de insuficiência renal dialítica ou transplante foi significativamente menor no grupo metilprednisolona do que no grupo placebo (50 [19,5%] vs 67 [27,2%]; HR, 0,59 [IC 95%, 0,40- 0,87]; P = 0,008; a diferença anual da taxa de eventos, **-2,9% ao ano** [IC de 95%, -5,4% a -0,3%] **(Figura B).**
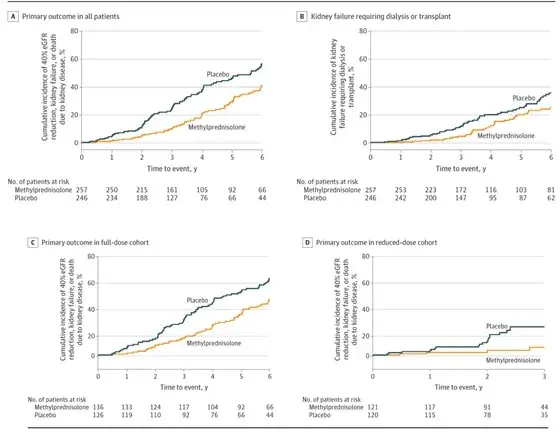
Após avaliar separadamente as duas coortes (alta e baixa dose) o benefício do uso do corticosteroide foi mantido.
A taxa anual de queda da TFGe foi de 2,50 mL/ min/1,73m2 por ano no grupo metilprednisolona comparado com 4,97mL/min/1,73m2 por ano no grupo placebo (diferença média, 2,46 mL/min/ 1,73 m2 por ano [IC 95%, 0,94-3,99]; P = 0,002.
Na análise de subgrupos, o efeito se manteve, com exceção da população **acima de 50 anos e com o benefício sendo maior na população não chinesa.**
Com relação aos efeitos colaterais, os eventos adversos graves (EAG) foram relatados em 28 participantes (10,9%) no grupo metilprednisolona em comparação com 7 (2,8%) no grupo placebo (tabela abaixo), principalmente devido ao excesso de internações (25 vs 7) e infecções graves (17 vs 3).
O **excesso de eventos** foi principalmente observado com o regime de dose completa de metilprednisolona em comparação com participantes randomizados para receber placebo durante esse período de estudo (22 vs 4), em vez do regime de dose reduzida em comparação com os participantes no grupo placebo randomizado naquele momento (6 vs 3). Quatro eventos adversos graves foram fatais, todos os quais estavam na grupo metilprednisolona (1,6%) e relacionados à infecção, incluindo 3 no protocolo de dose elevada (2,2%) e 1 no protocolo de dose deduzida (0,8%).
Neste ensaio clínico randomizado de pacientes com NIgA e proteinúria > 1 g por dia, a o tratamento com metilprednisolona por 6-9 meses, em comparação com o placebo, reduziu significativamente o risco de resultado composto de declínio na função renal, doença renal crônica dialítica/transplante ou morte devido a doença renal.
No entanto, o incidência de eventos adversos graves aumentou com metilprednisolona e o regime de dose reduzida tiveram menos eventos adversos em comparação com o regime de dose completa.
No geral, esses dados sugerem que um curso de 6 a 9 meses de terapia oral corticosteróides efetivamente protegeram a função renal em pessoas com NIgA e que esse benefício pode ser realizado com um protocolo de dose reduzida com menor risco de eventos adversos.
Embora este estudo tenha incluído uma grande porcentagem de participantes da China, para quem diferentes prognósticos e/ou resposta terapêutica foram propostas, não houve evidência de perda de eficácia no benefício renal em pacientes não chineses.
O aumento do risco de infecções foi mitigado com a redução da dosagem e adição de profilaxia antibiótica com sulfametoxazol-trimetoprima, tal que uma menor incidência de efeitos adversos graves eventos foram observados nos grupos de dose reduzida após esses mudanças foram feitas.
Este estudo foi o maior estudo em NIgA até o momento e forneceu evidências mais precisas do que ensaios anteriores sobre os benefícios e riscos deste tratamento. A natureza duplo-cega da intervenção, bem como o longo e rigoroso acompanhamento reduziu o risco de viés, e por ser o multicêntrico e internacional aumentou seu poder de generalização.
Porém, a maioria dos participantes eram da China. A dose de metilprednisolona usada no protocolo original aumentou o risco de eventos adversos e o ensaio foi modificado.
## OPINIÃO NEFROATUAL
Após estes estudos fica mais claro que a terapia imunossupressora tem seu efeito benéfico, seja na proteinúria, na progressão da disfunção renal e em desfechos duros, como início de TRS e morte por causa renal. Porém, os riscos da terapia não são nulos e devemos fazê-lo com cuidado, especialmente, para pacientes com comorbidades associadas.
Pacientes com **TFGe <30mL/min**, **diabéticos**, **obesos**, com **osteoporose** e com **infecções latentes** não devem ser submetidos ao tratamento com esteroides de acordo com o KDIGO 2021 de glomerulopatias. Neste caso, pode ser adicionado iSGLT2.
Nos estudos randomizados em que os imunossupressores foram utilizados, não foi avaliado o uso dos iSGLT2 pré randomização. Acreditamos que a adição desta classe de medicamentos aos IECA/BRA pode diminuir o número de pacientes com alto risco, e pode ser uma estratégia utilizada antes do uso dos imunossupressores.
Para pacientes com proteinúria acima de 1g, realizamos o esquema com dose reduzida, conforme feito no **TESTING trial 2022** (mas usamos a prednisona 0,5mg/kg até o máximo de 40mg/d, com desmame de 5 mg ao mês).
Já existem outras terapias como budesonida oral, inibidores de endotelina e anticorpos monoclonais mais seguras e que podem ser adicionadas à terapia padrão com IECA/BRA e iSGLT2. Quem sabe teremos estudos com terapias combinadas em breve?
E você? Usa a dose reduzida de corticoide na IgA?
 Paciente em Diálise Engravidou: Como Conduzir com Segurança?
Paciente em Diálise Engravidou: Como Conduzir com Segurança?

 Qual o limite para o consumo de proteína sugerido pelo KDIGO de DRC 2023?
Qual o limite para o consumo de proteína sugerido pelo KDIGO de DRC 2023?