Nos últimos anos, as terapias alvo moleculares têm revolucionado o tratamento de neoplasias, melhorando significativamente a sobrevida de pacientes com diferentes tipos de câncer. Essas terapias atuam interferindo em alvos moleculares específicos relacionados ao crescimento tumoral. Contudo, muitos desses alvos também estão presentes em células normais, como as renais, o que torna os efeitos adversos renais uma preocupação crescente. A seguir, baseado no artigo publicado no Kidney360 ([link](https://journals.lww.com/kidney360/pages/articleviewer.aspx?year=2024&issue=11000&article=00022&type=Fulltext)), revisamos como diferentes classes de terapias alvo moleculares podem causar injúria renal aguda (IRA) e discutimos estratégias de manejo.
Antes de tudo vale a pena conferir a tabela abaixo para entender os tipos de terapias alvo moleculares:
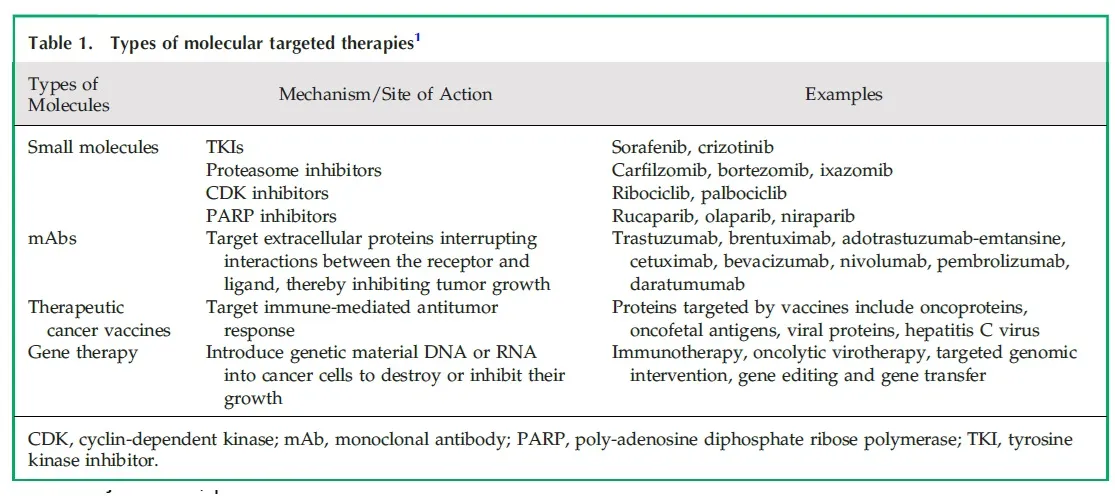
Agora vamos falar pontos importantes para os nefrologistas dos principais agentes:
##### 1-Inibidores de VEGF/VEGFR
Esses medicamentos, como o bevacizumabe (anticorpo monoclonal) e os inibidores de tirosina quinase (sunitinibe, cabozantinibe, lenvatinibe e axitinibe), revolucionaram o tratamento de tumores como carcinoma de células renais e câncer colorretal. No entanto, são associados a alterações na microvasculatura renal, hipertensão e, em alguns casos, microangiopatia trombótica (MAT).
Abordagem terapêutica: Controle rigoroso da pressão arterial, preferencialmente com inibidores da enzima conversora de angiotensina ou bloqueadores dos receptores da angiotensina. A proteinúria leve não requer a suspensão da medicação, mas casos graves (síndrome nefrótica, MAT ou IRA) podem exigir interrupção do tratamento.
##### 2-Inibidores de FGFR
A inibição do receptor do fator de crescimento de fibroblastos (FGFR) pode levar a hiperfosfatemia em até 74% dos pacientes, frequentemente relacionada à desregulação da homeostase do fósforo. O erdafitinibe é um exemplo dessa classe.
Abordagem terapêutica: Dieta com restrição de fósforo e uso de quelantes de fósforo em casos de níveis superiores a 7 mg/dL. Casos graves, como calcifilaxia, podem exigir redução de dose ou suspensão do medicamento.
##### 3-Inibidores de Tirosina Quinase
Os inibidores de tirosina quinase (ITQ) possuem ampla aplicação em neoplasias, como leucemia mieloide crônica e carcinoma renal. A toxicidade renal depende do alvo molecular:
* cMET (ex.: crizotinibe): Nefropatia obstrutiva por cristais.
* FLT3 (ex.: gilteritinibe): IRA pré-renal associada à diarreia.
* EGFR (ex.: erlotinibe, gefitinibe): Lesões variadas, como nefropatia por IgA, nefrite intersticial aguda e necrose tubular aguda.
* Multi-ITQ (ex.: imatinib, sunitinibe, ceritinib, crizotinibe): Relatados como causadores de cistos renais complexos que podem exigir acompanhamento clínico ou drenagem. Também estão associados a IRA pré-renal e anormalidades eletrolíticas. O ceritinib, em particular, pode causar hipofosfatemia em 10% dos pacientes, hipomagnesemia em 8% e elevação da creatinina em 11%. Além disso, há casos de pseudo-IRA por redução da secreção tubular de creatinina, sendo essencial verificar os níveis de cistatina C para diferenciar de uma IRA verdadeira.
Abordagem terapêutica: Ajustes de dose ou suspensão do medicamento conforme a gravidade da toxicidade, com foco em suporte clínico.
##### 4-Inibidores de Tirosina Quinase Treonina/Serina
* Inibidores de BRAF (ex.: vemurafenib): Usados no tratamento de melanoma metastático, podem causar nefrite intersticial aguda, frequentemente nas primeiras semanas de tratamento.
* Inibidores de CDK 4/6 (ex.: ribociclib): Associados a IRA em até 60% dos pacientes, com necrose tubular aguda como a principal manifestação. O abemaciclib pode causar pseudo-IRA por inibição da secreção tubular de creatinina.
##### 5-Inibidores de Proteassoma
O bortezomibe e o carfilzomibe são amplamente usados em neoplasias hematológicas e podem causar MAT ou nefrite intersticial aguda granulomatosa.
Abordagem terapêutica: Pode ser necessária a suspensão do medicamento e, nos casos de NIA, uso de corticosteróides.
##### 6-Inibidores de BCL-2
O venetoclax, utilizado para leucemia linfoide crônica e leucemia mieloide aguda, está associado a altas taxas de síndrome de lise tumoral. O risco é maior em pacientes com alta carga tumoral ou quando a dose inicial é elevada.
Abordagem terapêutica: Profilaxia com medicamentos hipouricemiantes e hidratação antes do início do tratamento.
##### 7-Inibidores Epigenéticos
Os inibidores de histona desacetilase (ex.: romidepsina) e de DNA metiltransferase (ex.: decitabina, azacitidina) são usados em neoplasias hematológicas.
* Romidepsina: Pode induzir glomeruloesclerose segmentar e focal colapsante, que pode ser tratada com corticosteróides e suspensão da medicação.
* Azacitidina e decitabina: Associadas a lesão tubular proximal, síndrome de Fanconi e pseudo-IRA, geralmente reversíveis com a suspensão do medicamento.
##### 8-Inibidores de PARP
Medicamentos como olaparibe e niraparibe, usados no tratamento de cânceres com mutação no gene BRCA, podem causar pseudo-IRA ao inibir a secreção tubular de creatinina.
Abordagem terapêutica: Caso confirmada a pseudo-IRA, a elevação da creatinina é benigna e não requer descontinuação do tratamento.
##### Importância dessa nova terapia para os Nefrologistas:
A rápida evolução das terapias alvo moleculares destaca a necessidade de que nefrologistas estejam familiarizados com os mecanismos de nefrotoxicidade dessas drogas. Identificar precocemente e manejar adequadamente os efeitos renais permite melhorar a segurança e a eficácia do tratamento oncológico. A colaboração interdisciplinar entre oncologia e nefrologia é fundamental para garantir melhores desfechos clínicos e minimizar complicações renais em curto e longo prazo.
 Agonista GLP-1 em Comprimido: A Semaglutida Oral Reduz Eventos CV em Pacientes com DM2 e DRC?
Agonista GLP-1 em Comprimido: A Semaglutida Oral Reduz Eventos CV em Pacientes com DM2 e DRC?


 A Importância do Exercício Físico na Preservação da Função Renal em Idosos
A Importância do Exercício Físico na Preservação da Função Renal em Idosos